Caractéristiques et utilisation comme édulcorant
Le cyclamate de sodium a été synthétisé pour la première fois en 1937 par un étudiant au doctorat de l’Université de l’Illinois, Michael Sveda, qui avait accidentellement découvert son goût sucré. Le brevet de production de cyclamate de sodium est devenu la propriété des laboratoires Abbott, qui ont effectué les études nécessaires pour pouvoir l’utiliser comme édulcorant sans danger. Dans les années 1960, la consommation de cyclamate aux États-Unis est montée en flèche, car il est devenu populaire pour adoucir les «boissons sans alcool» mélangées à la saccharine. Cependant, l'aspect lié à sa toxicité fait encore l'objet de nombreuses discussions et certains pays, dont les États-Unis eux-mêmes, ont interdit son utilisation dans l'alimentation.
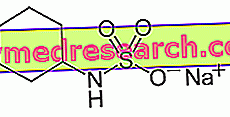
Les cyclamates dérivent des sels de sodium et de calcium de l'acide cyclique. L'acide cyclique, ou acide cyclohexylsulfamique, est une poudre cristalline blanche ayant un point de fusion (169-170 ° C), une bonne solubilité (1 g / 7, 5 ml) et un goût acidulé. C'est un acide fort. Le pH d’une solution à 10% est d’environ 0, 8-1, 6. Les dérivés de sodium (cyclamate de sodium) et de calcium (cyclamate de calcium) sont des électrolytes puissants, ils sont donc fortement ionisés en solution. Les deux sels existent sous forme de cristaux ou de poudres cristallines blanches. Ils sont très solubles dans l’eau (1 g / 4 à 5 ml), mais pas dans l’huile et les solvants apolaires. Les cyclamates sont stables à la lumière, à la chaleur et dans une large gamme de pH.
La cyclohexylamine est le composé dont dérivent l'acide cyclique et ses sels; c'est aussi le produit de leur métabolisme et possède des propriétés complètement distinctes, certaines toxiques (voir ci-dessous).
Le cyclamate, contrairement au saccharose (goût sucré immédiat, intense, propre), a un goût sucré retardé, mais très persistant; il est considéré environ 30 fois plus sucré que le saccharose, mais son pouvoir sucrant relatif a tendance à diminuer avec la concentration. Cette caractéristique peut être expliquée en partie par l'arrière-goût et le goût amer perçus à des concentrations élevées. Les sels de calcium sont considérés comme moins sucrés que le sodium, et les problèmes d’arrière-goût et de goût désagréable (goût désagréable) se font déjà sentir à des concentrations inférieures à celles du sel de sodium et de l’acide.
Le cyclamate est principalement utilisé comme édulcorant non calorique, généralement en association avec d'autres édulcorants, mais il peut également être utilisé comme agent aromatisant (pour masquer le goût des médicaments). Dans les pays où l'utilisation est autorisée, il est utilisé comme édulcorant en poudre ou en comprimés ou sous forme liquide, dans les boissons et jus de fruits, dans les produits à base de fruits, dans les chewing-gums et les bonbons (c'est un acariogène), dans les codages, gelées confitures et nappages.
Le cyclamate de sodium est autorisé dans 50 pays, dont l’Italie, avec quelques limitations. La DJA varie d'un pays à l'autre et se situe autour de 0-11 mg / kg de poids corporel. Le poids en mg est relatif à l'acide cyclique.
Le cyclamate est généralement utilisé en mélange avec d'autres édulcorants et en particulier avec la saccharine. Dans ce mélange, le goût est inexistant et le pouvoir sucrant est fortement accru: au moins 10 à 20% de l'effet synergique a été observé lorsque la saccharine et le cyclamate de sodium sont utilisés ensemble. Par exemple, 5 mg de saccharine et 50 mg de cyclamate mélangés sont aussi sucrés que 125 mg de cyclamate seul ou 12, 5 mg de saccharine seule. Habituellement, le rapport utilisé dans ces mélanges cyclamate / saccharine est de 10: 1, car avec cette combinaison, chaque composant contribue également au pouvoir édulcorant (car la saccharine est environ 10 fois plus sucrée que le cyclamate). Certaines applications plus récentes voient le cyclamate de sodium avec l'aspartame ou l'acésulfame K ou encore en combinaison ternaire avec la saccharine et l'aspartame.
Le cyclamate de sodium présente un certain nombre de qualités techniques qui le rendent utilisable comme édulcorant de remplacement. Ce n'est pas calorique et n'est pas cariogène. Bien que son pouvoir édulcorant soit inférieur à celui de la saccharine et de l'aspartame, il convient à une utilisation en tant qu'édulcorant, en particulier en combinaison avec d'autres édulcorants. À des concentrations normales, le profil gustatif est favorable et renforce les arômes de fruits; il est compatible avec de nombreux aliments, ingrédients, arômes naturels et artificiels, autres édulcorants, conservateurs chimiques. La solubilité dans l'eau est excellente, ainsi que la stabilité à des températures basses et élevées, à différents pH et en présence de lumière et d'oxygène. Il n'est pas hygroscopique et ne favorise pas la croissance des champignons et des bactéries.
Sécurité d'utilisation et effets secondaires
Le cyclamate de sodium est absorbé lentement et de manière incomplète le long du tractus gastro-intestinal. Dans une étude portant sur environ 200 sujets, l'absorption de cyclamate était en moyenne de 37%. Une fois absorbé, le cyclamate de sodium ne se concentre pas dans les tissus et est excrété avec l'urine non métabolisée. Des études supplémentaires ont montré que chez certains individus, y compris l'homme, le cyclamate de sodium peut être métabolisé en cyclohexylamine, bien que dans des pourcentages très variables d'un sujet à l'autre, chez le même individu à des moments différents, dans les différents pays du monde, etc.
Le cyclamate de sodium n'est pas métabolisé par les tissus, mais la cyclohexylamine se forme à la suite de la microflore du cyclamate de sodium non absorbé le long du tractus intestinal. Le cyclamate a longtemps été étudié pour sa cancérogénicité présumée sur la vessie de rat. Le problème est similaire à celui de la saccharine et, en fait, les études ont été menées principalement en ce qui concerne l'association des deux édulcorants. Il y a encore beaucoup de pentes concernant sa toxicité, mais aucune preuve directe réelle. Aux États-Unis, l’utilisation du cyclamate de sodium est toujours interdite. Le métabolite de la cyclohexylamine est considérablement plus toxique et c’est précisément cette toxicité qui limite l’utilisation du cyclamate comme édulcorant; de nombreuses études sont encore en cours, mais les deux principaux domaines de problèmes de toxicité sont liés aux effets cardiovasculaires et à l’atrophie testiculaire.